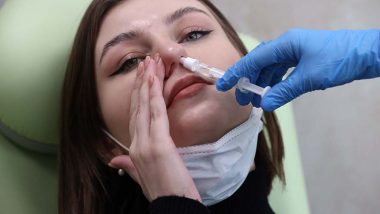
औषध नियामकांनी भारतातील पहिल्या इंट्रानासल म्हणजे (Intranasal Vaccine) नाकाद्वारे कोविड-19 (Covid - 19) लसीसाठी मानवी चाचण्यांच्या दुसऱ्या टप्प्याला परवानगी दिली आहे. भारत बायोटेक (Bharat Biotech) सेंट लुईसच्या वॉशिंग्टन विद्यापीठाच्या सहकार्याने कोविड-19 लस म्हणजेच BBV154 विकसित करत आहे. केंद्रीय विज्ञान आणि तंत्रज्ञान मंत्रालयाने सांगितले की, इंट्रानासल रिप्लिकेशन-डेफिसिएंट चिंपांझी एडेनोव्हायरस SARS-CoV2 व्हेक्टर लस ही भारतातील नियामक मान्यता मिळवणारी पहिली लस ठरली नाही, तर भारतातील मानवी चाचण्यांमधून होणारी ही पहिलीच लस आहे. तसेच मंत्रालयाने सांगितले की, भारत बायोटेकला SARS-CoV-2 लसीच्या विषम (वेगळ्या परंतु संबंधित प्रजातींपासून मिळालेल्या) प्राइम बूस्ट कॉम्बिनेशनसह BBV152 ची कार्यक्षमता आणि सुरक्षितता तपासण्यास सांगितले आहे.
चाचणीमध्ये कोणतेही गंभीर प्रकरण दर्शविले गेले नाही
भारत बायोटेकने अलीकडेच 18-60 वर्षे वयोगटातील निरोगी स्वयंसेवकांवर चिंपांझी एडेनोव्हायरस लसीची फेज-1 चाचणी पूर्ण केली. मंत्रालयाचे म्हणणे आहे की, फेज-1 चाचणीत स्वयंसेवकांना दिलेला डोस त्यांनी चांगलाच सहन केला. कोणत्याही प्रकारचे गंभीर प्रकरण समोर आले नव्हते. पूर्वी, प्रयोगशाळेतील अभ्यासांमध्ये प्री-क्लिनिकल टॉक्सिसिटी अभ्यासामध्ये ही लस सुरक्षित, इम्युनोजेनिक आणि सहन करण्यायोग्य असल्याचे आढळून आले होते. प्राण्यांवरील अभ्यासात असे आढळून आले आहे की ही लस उच्च पातळीचे निष्प्रभावी प्रतिपिंड तयार करण्यास सक्षम आहे. (हे देखील वाचा: Covid Cases In India: तीन महिन्यांनंतर देशात कोरोना रुग्ण संख्या 4000 पार)
मंत्रालयाने सांगितले की जैवतंत्रज्ञान विभाग (DBT) आणि बायोटेक्नॉलॉजी इंडस्ट्री रिसर्च असिस्टन्स कौन्सिलच्या सहकार्याने इंट्रानासल लस विकसित करण्यात आली आहे. DBT सचिव आणि BIRAC प्रमुख डॉ. रेणू स्वरूप म्हणतात की भारत बायोटेकची BBV154 ही भारतात विकसित होणारी पहिली इंट्रानासल लस आहे जी तिच्या क्लिनिकल चाचण्यांच्या शेवटच्या टप्प्यात प्रवेश करण्याच्या स्थितीत आहे.

































